尺寸小于400纳米的纳米塑料能够穿透生物屏障并在组织中富集,这一现象正引发毒理学和公共卫生领域的广泛担忧。研究表明,这些超小颗粒可能诱发多系统毒性,包括脑和神经系统损伤、心血管功能障碍、生殖风险以及细胞和胃肠道毒性。要在血液或血清这样充满蛋白质、无机盐的复杂高粘度基质中精准大海捞针,找出痕量的纳米塑料,传统的分析手段往往显得力不从心。无论是耗时极长的样本前处理,还是对超微小颗粒缺乏足够的检测灵敏度,都构成了现阶段环境毒理学与临床评估的巨大技术阻碍。(如原文图1所示)
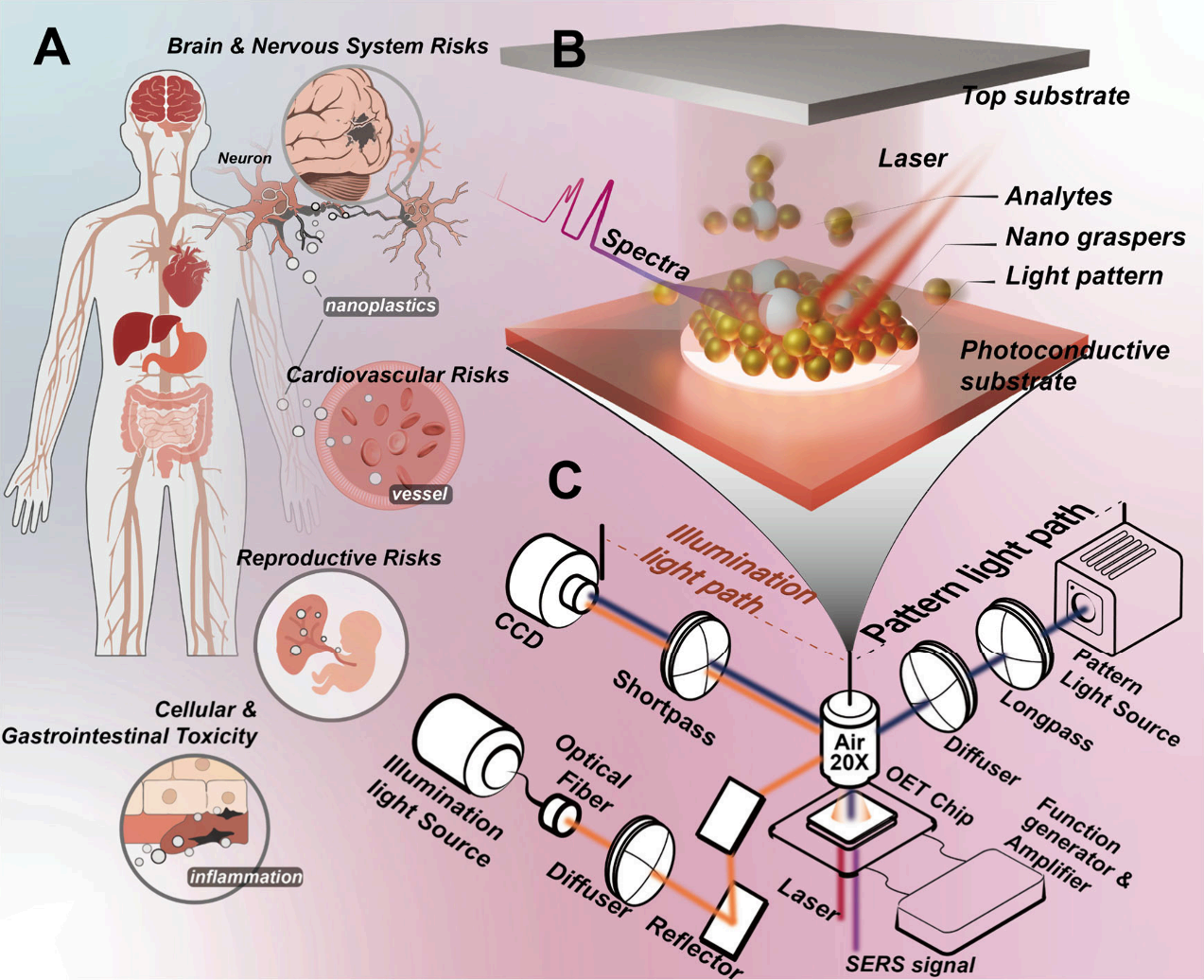
图 1 .(A) 纳米塑料对健康影响的示意图;(B) OET 芯片示意图,光图案引导纳米机械手捕获和富集目标分析物;(C) OET-NGP 平台的光学设置和系统配置,用于纳米颗粒操作和 SERS 检测。
近期,北京理工大学张帅龙教授及付荣鑫副研究员团队联合多位学者,在《ACS Nano》上发表了一项极具启发性的工作。他们设计了一种基于光电镊辅助的“纳米机械手”系统。该系统利用结构光引导光致交流电渗流(LACE)与介电泳(DEP)力的协同作用,在液相中动态组装金纳米颗粒形成“纳米机械手”,在10秒左右的时间内主动抓取并包裹目标纳米塑料,快速富集分析物,还能形成高度均匀的热点,从而生成高强度的表面增强拉曼散射(SERS)信号。这项工作巧妙地化解了复杂生物流体中痕量大分子和颗粒物检测的难题。
寻找完美SERS底物的技术折中
在纳米级分析物检测中,SERS技术凭借其分子级的指纹图谱识别能力获得了广泛青睐。在这个领域,研究人员始终面临一个核心矛盾:如何获得既高度均匀又具备极强信号放大能力的SERS热点。
传统的SERS平台通常分为两类。一类是胶体系统,将金属纳米颗粒悬浮在溶液中。这种方式成本低廉且易于高通量操作,但纳米颗粒在溶液中的随机分散往往导致信号极不稳定,在低浓度下极易产生不受控的聚集或吸附到不需要的表面。另一类是基于微纳加工的固体结构底物,它们提供了定义明确的SERS热点和出色的信号重现性。固态底物的设计和制造过程复杂耗时,静态的几何布局缺乏灵活性,难以追踪移动的分析物或根据样本条件的变化进行动态调整。
科研人员亟需一种兼具液态体系灵活性与固态体系稳定性的新一代探测平台。
技术机制解码:无形机械臂与可编程动态矩阵的完美协同
为解决上述困境,研究团队摒弃了传统的静态底物制备思路,转而开发了一种高度可重构的动态捕获系统。他们在实验中引入了光电镊(OET)技术,并巧妙利用光致交流电渗流(LACE)与介电泳(DEP)力的协同作用,实现了液相中金属纳米颗粒的精准操控。
整个实验的核心硬件依托于追光生物的OptoBot®500光电微流控系统。该平台集成了基于DMD的高精度结构光投影模块与灵活的电场控制单元。研究人员在OET芯片的液态层中均匀分散了直径60纳米的游离金纳米颗粒(AuNPs)。当系统施加15 kHz的交流偏置电压,并通过OptoBot ® 500向下层光电导薄膜(a-Si:H)投射特定形状的光图案时,光照区域的电导率迅速改变,局部电场发生重分布。(如原文图2所示)
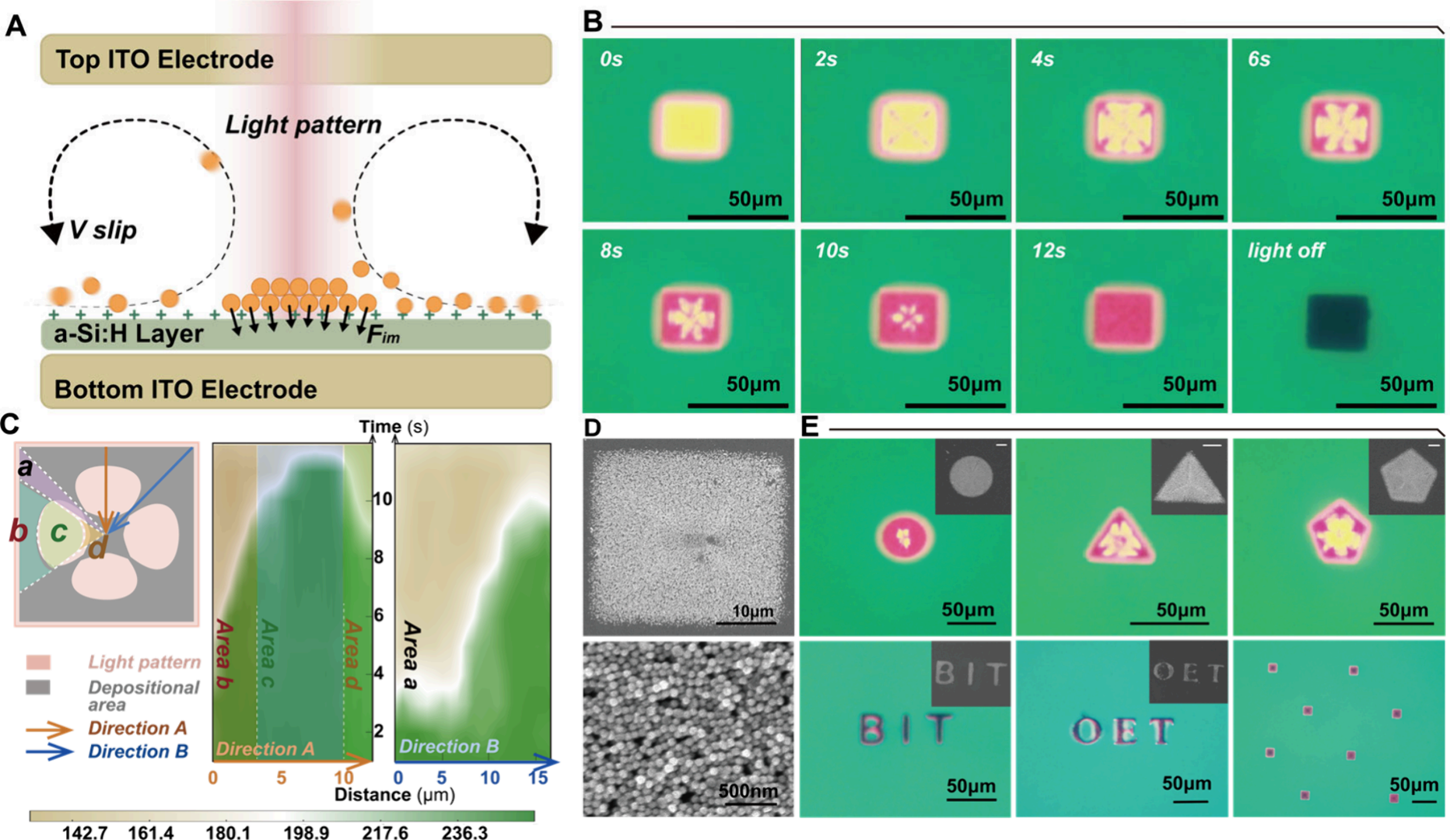
图2. (A) OET 芯片结构及其工作原理的横截面示意图,展示了光诱导力对纳米机械手的操作;(B) 时间序列图像,展示了矩形光图案下金纳米颗粒的聚集及其在基底上的固定;(C) 基于像素强度分析生成的时间相关灰度热图,展示了光照区域内两个方向上纳米颗粒聚集的演变;(D) 固定金纳米颗粒结构的扫描电子显微镜(SEM)图像,证实了高保真图案的形成;(E) 通过光控操作实现高精度、灵活组装成任意形状的演示。
这一过程触发了强烈的物理效应:光致电渗流在光照区域外围产生流体对流,将远处的游离金纳米颗粒和目标分析物源源不断地搬运到光照区边界;随之而来的强大介电泳力则像钉子一样,将这些颗粒牢牢固定在下层基底上。在显微镜下可以清晰地看到,原本游离的纳米颗粒在光图案的指引下,迅速向几何中心和顶点靠拢,最终致密排列成指定的形状。这种从边缘向中心蔓延的组装过程,宛如一只正在握紧的拳头,将周围的纳米塑料紧紧包裹在内,瞬间构建出大量具有极强颗粒间耦合效应的SERS热点。
突破性成果展示:从纯水介质到真实血清的跨越
这种动态组装策略在检测速度和灵敏度上展现了出色的数据表现。实验记录显示,仅仅需要约12秒,系统就能在芯片上完成一个30微米见方的致密纳米颗粒阵列的组装。
研究人员首先使用罗丹明B验证了系统的极限性能。校准曲线显示,罗丹明B的检测限(LOD)低至 4.43 × 10-8 M。更为关键的是信号的极高一致性:在单一“纳米机械手”结构内部,1505 cm-1 处特征峰强度的相对标准偏差(RSD)仅为8.11%;而在五个独立生成的结构之间,批次间RSD更是低至6.89%。这一数据完全达到了高质量商用SERS底物对信号波动的苛刻要求。(如原文图3所示)
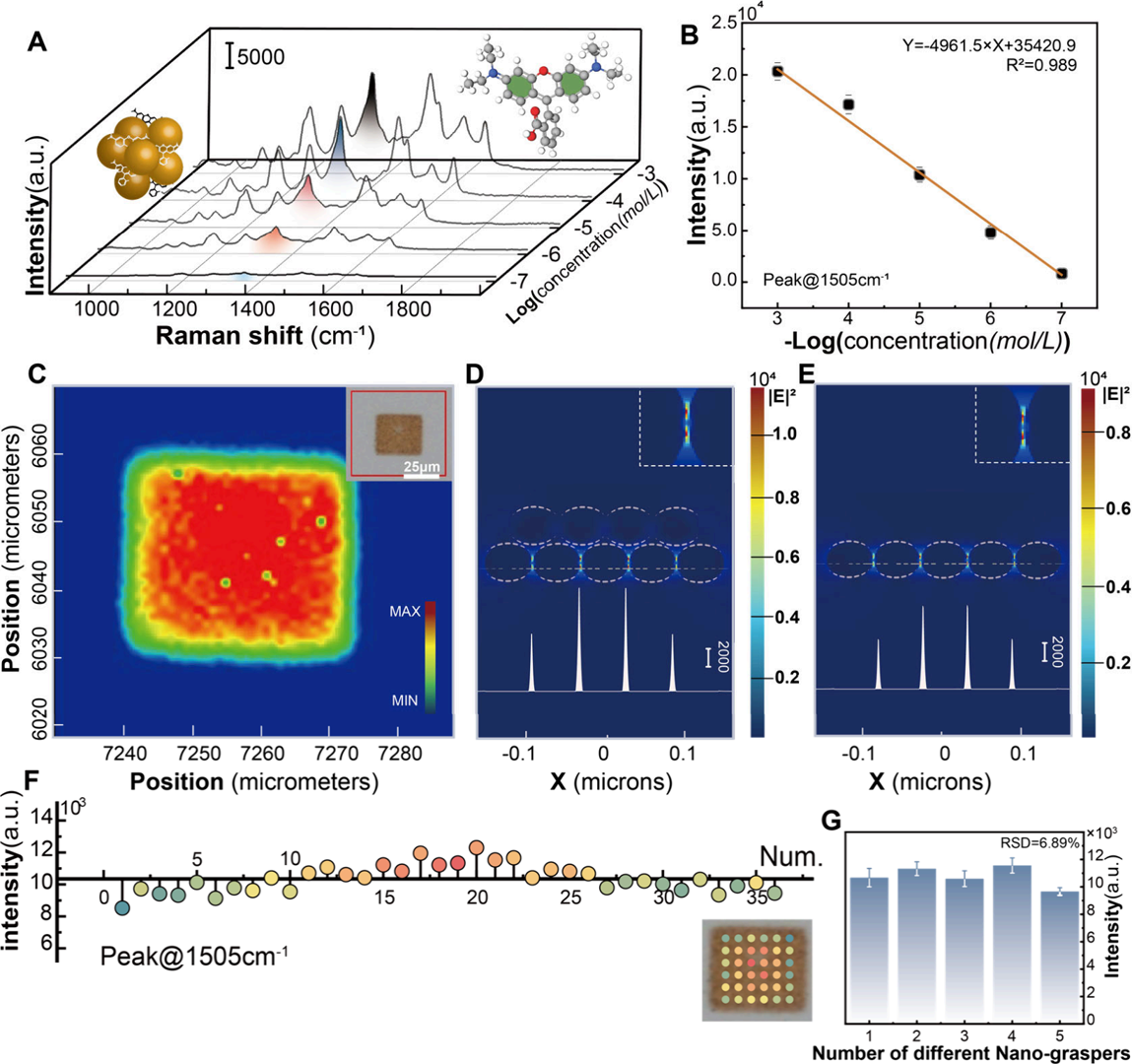
图 3. (A) 纳米机械手从溶液中捕获罗丹明B的拉曼光谱,浓度范围从10-3 M到10-7 M;(B) 罗丹明B的对数浓度与1505 cm-1处峰强度的线性拟合;(C) 纳米机械手在基底上沉积的拉曼映射图,展示了均匀性;(D) 多层纳米机械手结构的 FDTD 模拟电场强度分布;(E) 单层组装结构的 FDTD 模拟电场强度分布;(F) 单个纳米机械手图案内不同位置的1505 cm-1处拉曼峰强度,RSD为8.11%;(G) 五个不同纳米机械手的 SERS 峰强度比较,RSD为6.89%。
对于聚苯乙烯(PS)和聚对苯二甲酸乙二醇酯(PET)这两类代表性纳米塑料,该平台在纯水环境中的检测限分别达到了 5.6 μg/mL 和 8.9 μg/mL。这项工作最吸引人的突破在于对真实人类血清样本的直接检测。(如原文图4所示)
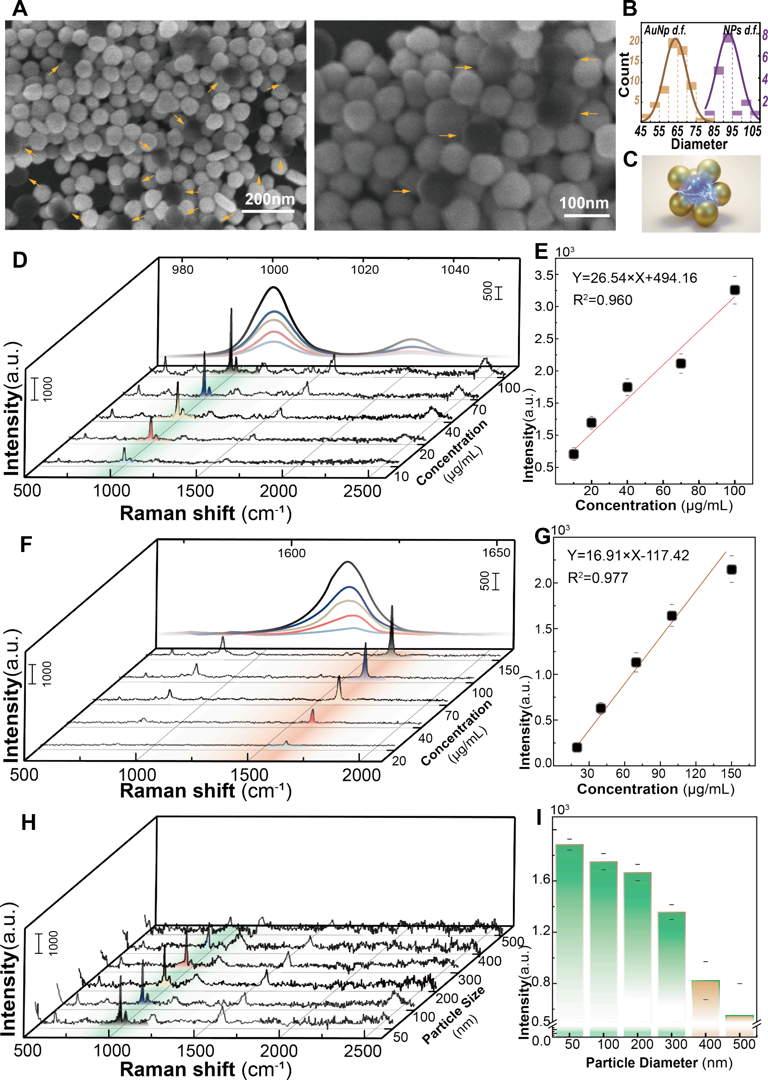
图 4. (A) 金纳米颗粒组装的纳米机械手包裹纳米塑料珠的 SEM 图像;(B) 金纳米颗粒和纳米塑料珠的尺寸分布;(C) 纳米机械手包裹纳米塑料颗粒产生 SERS 信号的示意图;(D) 不同浓度 PS 纳米塑料珠的 SERS 光谱;(E) 1003 cm-1处峰强度与 PS 珠浓度的校准曲线;(F) 不同浓度 PET 纳米塑料珠的 SERS 光谱;(G) 1614 cm-1处峰强度与 PET 珠浓度的校准曲线;(H) 不同尺寸 PS 纳米塑料的 SERS 光谱;(I) 不同尺寸 PS 纳米塑料在1003 cm-1处峰强度的比较。
血清样本具有极高的粘度、复杂的离子环境以及海量的背景生物大分子,这些因素极易干扰纳米颗粒的电动力学行为并引发非特异性沉淀。研究团队在OptoBot®500平台上开发了一种双步电压富集策略。在第一阶段施加15 V较低电压,利用低雷诺数下流体动力学的尺寸选择性,主要依靠交流电渗流将纳米机械手和纳米塑料温和地向光照区聚拢,避免大分子杂质的过早沉积。形成局部高浓度富集区后,迅速将电压切换至25 V,通过强化的介电泳力将富集复合物牢牢固定。
实验验证表明,尿酸等生物分子的背景信号保持在非常稳定的基线水平,牛血清白蛋白(BSA)和DNA等干扰物几乎不产生负面影响。为了进一步确证该方法的定量准确性,研究人员将其与行业标准的裂解气相色谱-质谱联用(pyGC-MS)进行了直接对比。结果非常直观:在10到20 μg/mL的低浓度区间,pyGC-MS由于血清基质的严重干扰出现了明显的定量偏差,而基于OET的“纳米机械手”SERS方法依然保持了极好的线性响应和信号一致性。(如原文图5所示)
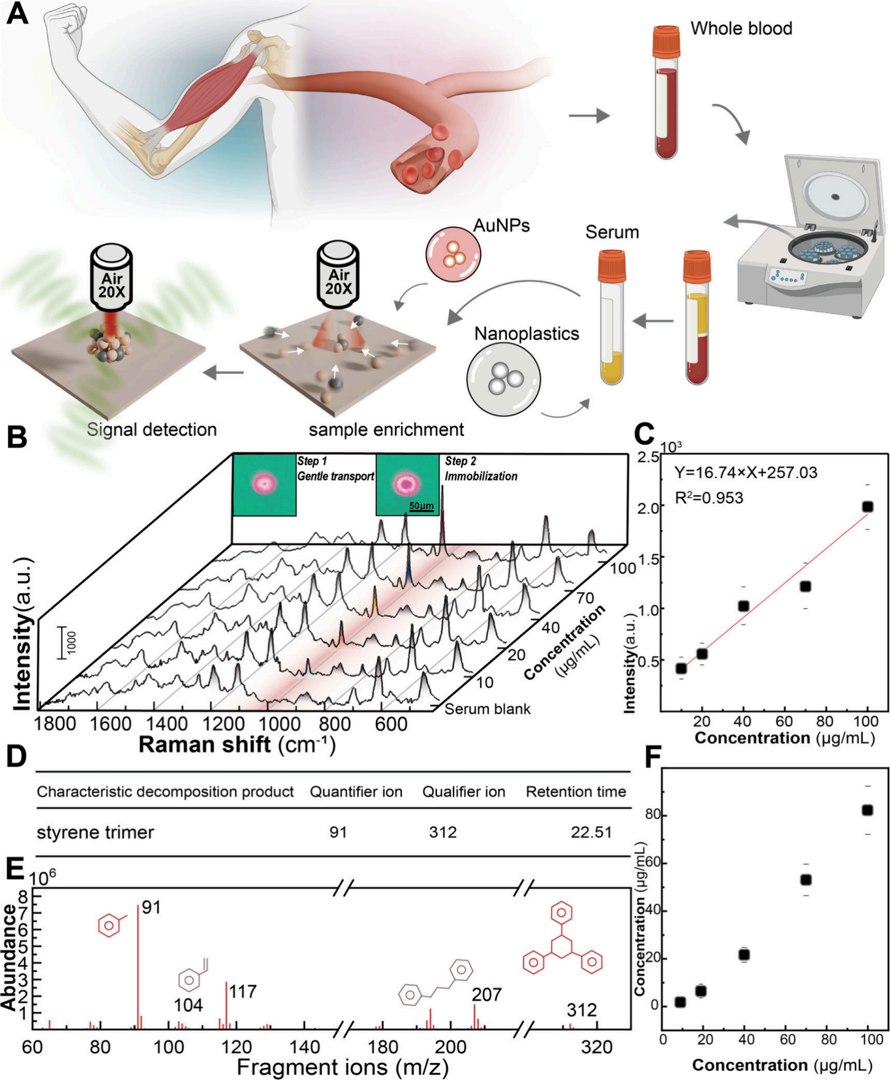
图 5.(A) 样品制备和检测工作流程的示意图;(B) 两步电压下血清中纳米机械手-纳米塑料复合物的富集过程示意图,以及不同纳米塑料浓度下的 SERS 光谱;(C) 峰强度与纳米塑料浓度的校准曲线,显示出良好的线性关系;(D) 所选特征离子(SSS)的二级质谱图,证实了纳米塑料成分的分子结构;(E) 加入纳米塑料的血清样品的 pyGC-MS 色谱图,显示了特征离子及其相应的保留时间,用于定性鉴定;(F) 所选离子信号强度与纳米塑料浓度的定量校准曲线,支持 SERS 定量结果。
方法学启示:变被动等待为主动富集
这项研究所展示的技术路线,为生化传感领域提供了一个全新的优化视角。
绝大多数高灵敏度光学检测都在被动等待靶标分子扩散到传感器表面。在极低浓度下,这种布朗运动带来的碰撞概率呈指数级下降,极大地拉长了检测周期。本研究利用光电微流控平台实现了真正意义上的“主动富集”。强大的局部流体漩涡将远处的靶标强行拉入检测区,彻底打破了扩散极限的物理瓶颈。
由于光照图案是完全可以通过软件实时定义的,研究人员在实验中轻松打出了三角形、六边形甚至“BIT”字母形状的SERS阵列。这种高度的空间可编程性意味着我们可以在同一微流控芯片上,针对不同区域的特定样本微环境,随时随地“按需打印”传感器,完成多位点平行测量。
当然,该技术方案目前也存在其特定的适用边界。研究表明,当目标塑料颗粒的直径超过400纳米时,拉曼信号强度会出现显著下降并伴随较高波动。这主要是因为微米级的大颗粒与60纳米的金颗粒之间存在尺寸不匹配,大颗粒难以被有效包裹进由小颗粒构建的紧密间隙中,导致热点密度降低。这一物理限制(尺寸匹配效应)明确了该技术目前的最佳应用场景:针对穿透性更强、毒理学意义更大的亚400纳米级微小颗粒物检测。
临床诊断与环境毒理学的新窗口
无论是微塑料在人体内的代谢追踪,还是液体活检中痕量外泌体、游离核酸的快速分析,对复杂生物流体的无前处理直接检测始终是生命科学仪器发展的高地。
结合高精度光控设备与纳米组装技术,研究团队成功将SERS的基底制备、靶标富集和信号读取压缩到了惊人的十几秒内。这种即插即用的动态传感理念,极大地简化了实验流程,降低了耗材成本。随着后续对靶向分离策略的进一步完善,这套基于光电微流控的“纳米机械手”平台,有望成为临床血液筛查和环境污染物毒性评估的标准实验工具之一,为下一代床旁检测(POCT)与高通量生物分析提供一条极具商业转化价值的技术捷径。
相关产品介绍:

追光生物OptoBot®500采用数字微镜器件(Digital Micromirror Device, DMD)投影技术,集成波形发生功能,无需搭配其他组件,即可完成对微纳目标的操控(金属颗粒、介电颗粒、纳米材料、细胞等)。集成操作软件OptoMind®500,通过软件编辑可实现图形编辑和微纳目标的运动控制。
参考文献: Wenbo Dong, Bingrui Xu, Rongxin Fu, et al. Light-Programmable Nanograspers for Rapid Nanoplastics Detection in Biological Fluids. ACS Nano (2026). DOI: 10.1021/acsnano.5c20989






 粤公网安备44030002004557号
粤公网安备44030002004557号
