在人体这台精密机器中,细胞之间时刻进行着海量的信息交换。它们专门使用一种微纳米级别的“快递包裹”——细胞外囊泡(Extracellular Vesicles, EVs,包含外泌体等)来进行沟通。囊泡内有蛋白质和核酸,其脂质双分子层外壳也富含生物信息,在免疫调控和肿瘤进展中发挥关键作用。然而,外泌体尺寸极小(30到150纳米),传统的超速离心捕获方法需消耗大量样本、耗时久,还易破坏囊泡活性,难以解决“大样本量需求”与“痕量珍稀样本获取”的矛盾。
近期,北京理工大学张帅龙教授团队联合多位学者在《Analytical Chemistry》上发表了一项巧妙的解决方案。他们构建了数字微流控与质谱联用(DMF-MS)平台,打造了一个全自动的微型化“外泌体分拣与开箱流水线”,实现了微升量级极微样本中细胞外囊泡的极速富集与原位脂质提取。这项技术成功将外泌体的富集与脂质提取时间从2小时以上压缩至短短15分钟,并实现了对微升量级极微样本的深度解析。
技术机制解码:让水滴在芯片上跳舞,告别繁琐的离心管
要突破传统前处理的通量与体积瓶颈,研究团队彻底抛弃了试管和移液器,转而将视线投向了数字微流控(DMF)技术。
这项研究巧妙地借助了基于介电润湿原理(EWOD)的数字微流控平台(其底层技术与追光生物的DropletBot®数字微流控系统高度一致)。在这类芯片上,微升甚至纳升体积的液滴被视作一枚枚可以自由移动的“棋子”。通过可编程的底层电极阵列切换电场,系统能够极其精准地控制液滴的生成、移动、合并与分离。(如原文图1所示)
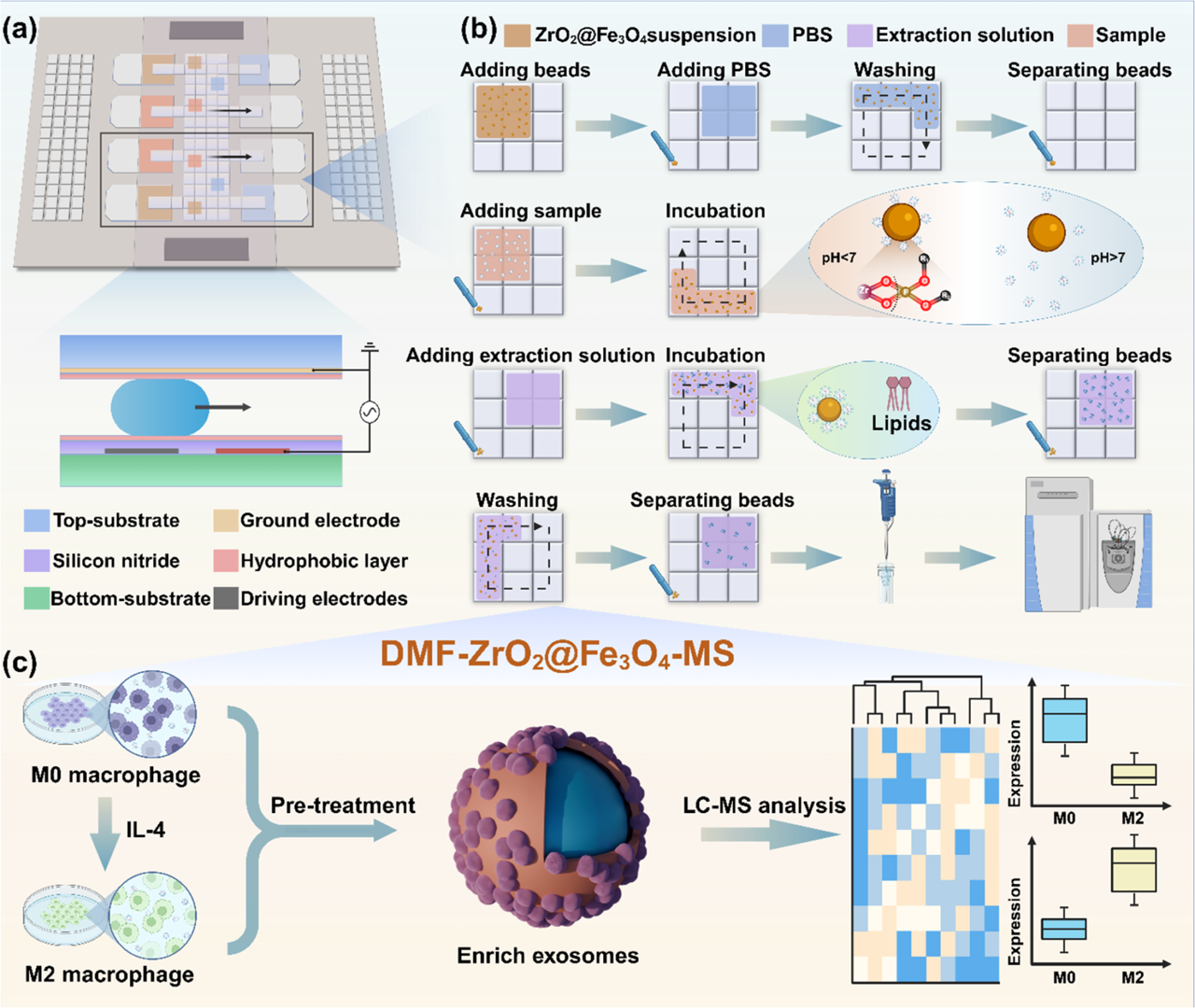
图1. (a) DMF 芯片结构;(b) EV 富集和脂质提取的详细工作流程;(c) 用于样品预处理和下游分析的一体化 DMF 策略。
为了在这些移动的水滴中精准“钓”出外泌体,研究人员设计了一种特制的“微观鱼钩”:表面包被二氧化锆的磁性纳米颗粒(ZrO2@Fe3O4)。这种设计的巧妙之处在于化学键的特异性识别。外泌体的脂质双分子层表面富含磷酸基团,而二氧化锆表面带有Zr4+路易斯酸性位点。当包裹着磁珠的液滴与样本液滴在芯片上合并时,Zr4+就像魔术贴一样,迅速且特异性地与外泌体表面的磷酸基团结合。(如原文图2所示)
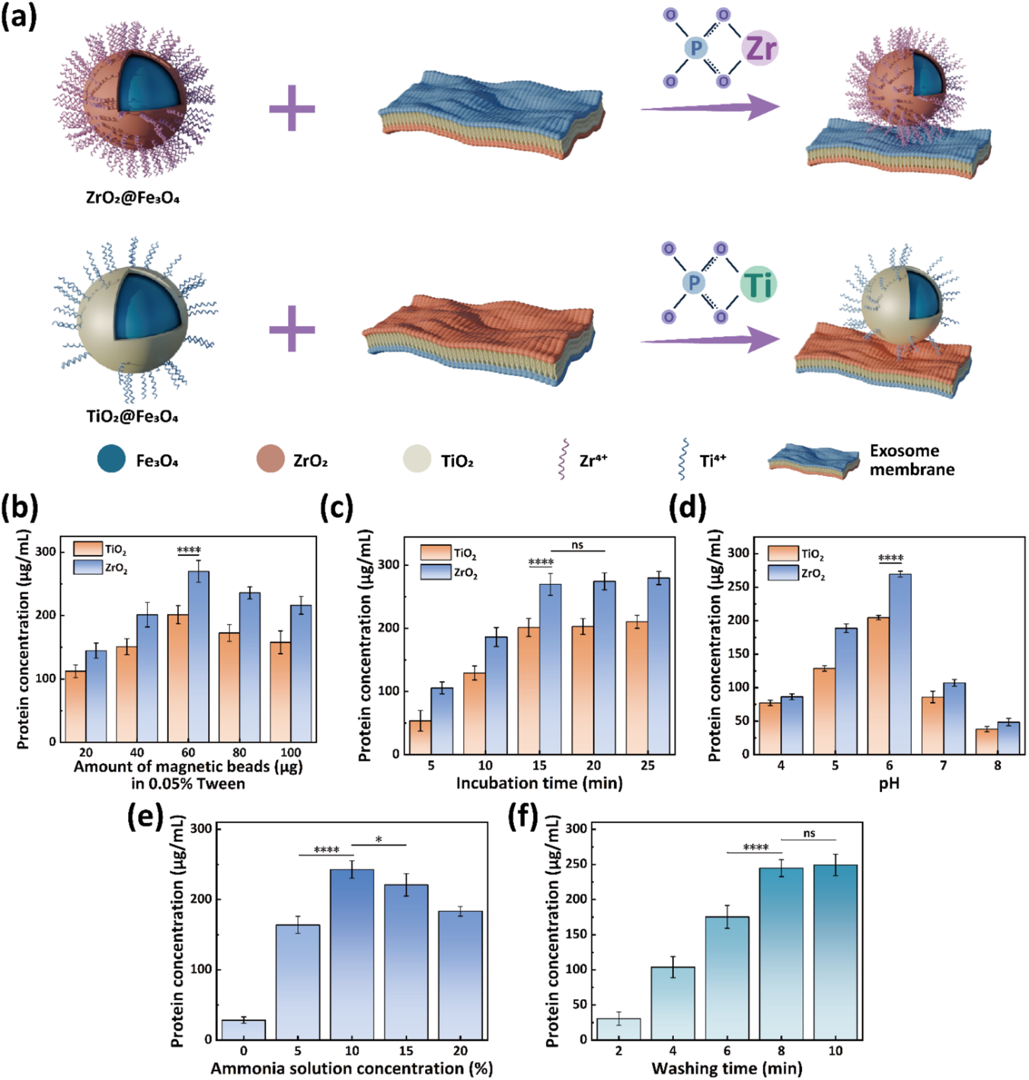
图2. (a) 使用 ZrO2@Fe3O4 和 TiO2@Fe3O4 磁珠进行 EV 富集的化学机制示意图;(b - d) 磁珠、孵育时间和溶液 pH 对 EV 富集效率的影响;(e, f) 氨浓度和洗脱时间对 EV 洗脱效率的影响。
在这个微型“加工厂”里,捕获、清洗、提取的完整生化反应全部在液滴内部闭环完成。包含外泌体和磁珠的液滴会在电场驱动下沿着设定路线来回移动,确保充分混合。随后,系统引入新的清洗液滴洗去杂质蛋白,最后直接在芯片上加入氯仿和乙腈的混合液滴进行原位脂质提取。整个过程封闭、自动化,彻底免除了人工移液带来的样本吸附损耗和交叉污染风险。
突破性成果展示:15 分钟,从微升量级(<2.5 μL)的稀缺样本中深度解析脂质图谱
极具创新的系统设计带来了令人瞩目的实验数据。
在富集效率上,只需使用极少量的样本(不足2.5微升),DMF-ZrO2@Fe3O4策略在15分钟内即可实现78%的外泌体回收率。虽然超速离心法(UC)需耗时 4 小时以上且回收率仅为约 42%,但DMF-ZrO2@Fe3O4策略在 15 分钟内即可实现 78% 的高回收率,实现了效率与性能的双重跨越。更重要的是,细胞划痕实验证实,这种温和的液滴内富集方式最大程度地保留了外泌体的生物学活性,其促细胞迁移的能力显著优于超速离心组。(如原文图3所示)
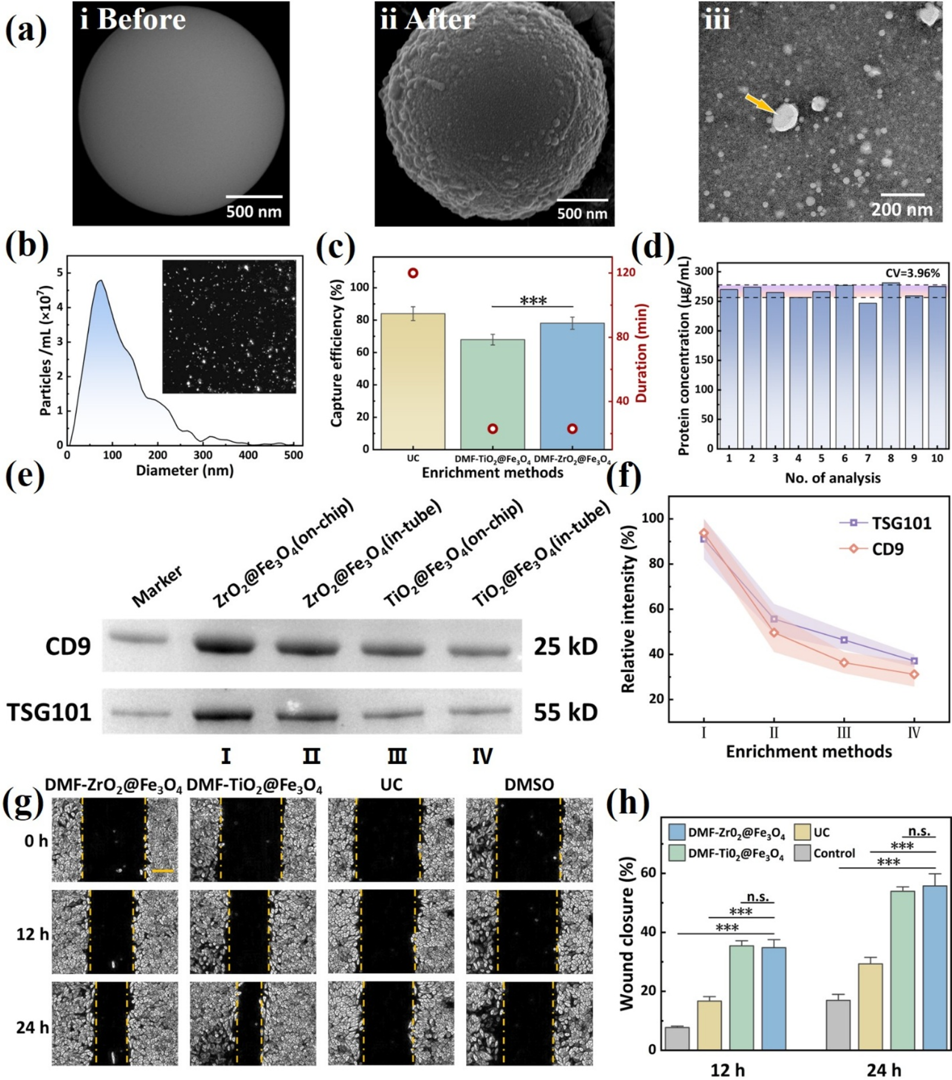
图 3.(a) DMF 芯片上与 EV 样本孵育前(i)和孵育后(ii)ZrO2@Fe3O4 磁珠的 SEM 图像,以及洗脱囊泡的 TEM 图像(iii),箭头指向杯状 EV;(b) 分离 EV 的 NTA;(c) 使用不同方法进行 EV 富集的回收率和所需时间的比较;(d) 使用 DMF-ZrO2@Fe3O4 方法进行 EV 富集的重现性分析;(e, f) 使用 ZrO2@Fe3O4 或 TiO2@Fe3O4 在芯片上或管中分离的 EV 中 CD9 和 TSG10l 的 Western blot 分析;(g) 使用不同方法富集的 EV 添加到培养基中用于 HeLa 细胞划痕实验;(h) 通过计算 12 或 24 小时划痕宽度与 0 小时划痕宽度的比值来确定 HeLa 细胞的划痕愈合率。
通过将芯片上提取的液滴直接送入质谱(MS)分析,研究团队在HeLa细胞衍生的外泌体中成功鉴定出349种脂质分子,比传统的Bligh-Dyer提取法多出近百种。这些脂质涵盖了甘油磷脂、鞘脂和甘油脂等多种类别,充分证明了该微型化平台在非靶向脂质组学分析中的强大覆盖能力。(如原文图4所示)
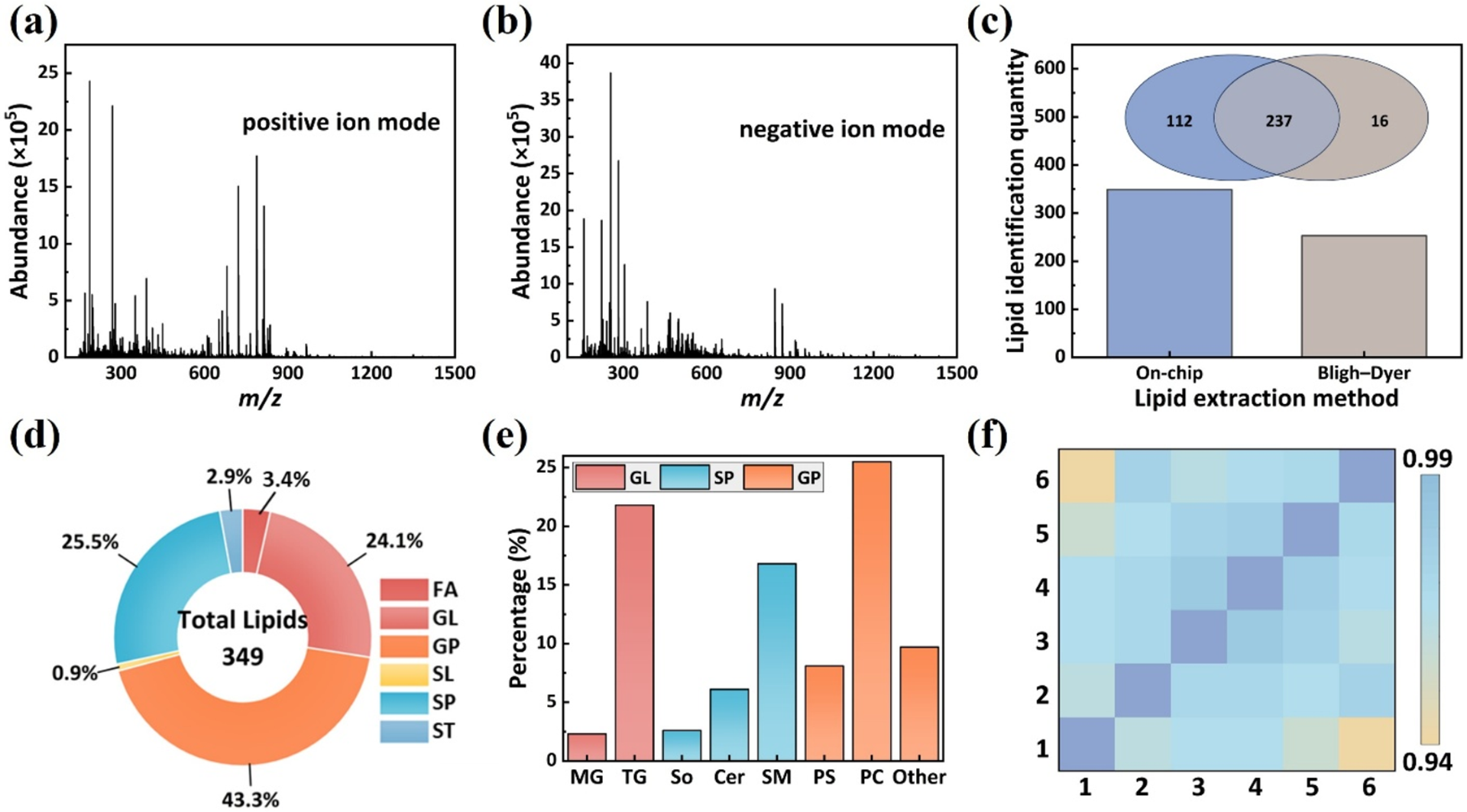
图 4.(a, b) 正离子和负离子模式下提取的外泌体脂质的质谱图;(c) 芯片提取与经典 Bligh−Dyer 方法之间脂质鉴定数量的比较;(d) 从 HeLa 细胞富集的 EV 中鉴定出的脂质的分类;(e) 从 HeLa 细胞富集的 EV 中鉴定出的脂质的亚分类;(f) 重复实验之间脂质丰度的相关性分析。
破译巨噬细胞的“维和部队”密码
为了验证该技术在复杂真实场景下的战斗力,研究人员将其应用于免疫学中一个极具挑战的课题:巨噬细胞极化状态的外泌体脂质分析。
巨噬细胞是免疫系统中的“清道夫”,主要分为处于静息状态的M0型和具有抗炎、促进组织修复功能的M2型。然而,获取特定极化状态的巨噬细胞及其分泌物极为困难,样本量往往非常稀缺。
借助这一全新的数字微流控质谱平台,研究人员对M0和M2两种状态的巨噬细胞外泌体进行了精准的脂质图谱比对。数据揭示了一个非常有趣的生物学现象:与静息状态的M0相比,M2型巨噬细胞分泌的外泌体中,具有抗炎特性的单不饱和脂肪酸(如棕榈油酸)和Omega-3脂肪酸(如DHA)的丰度出现了极其显著的上调;而作为细胞内脂质储存形式的胆固醇酯则大幅下降。(如原文图5所示)
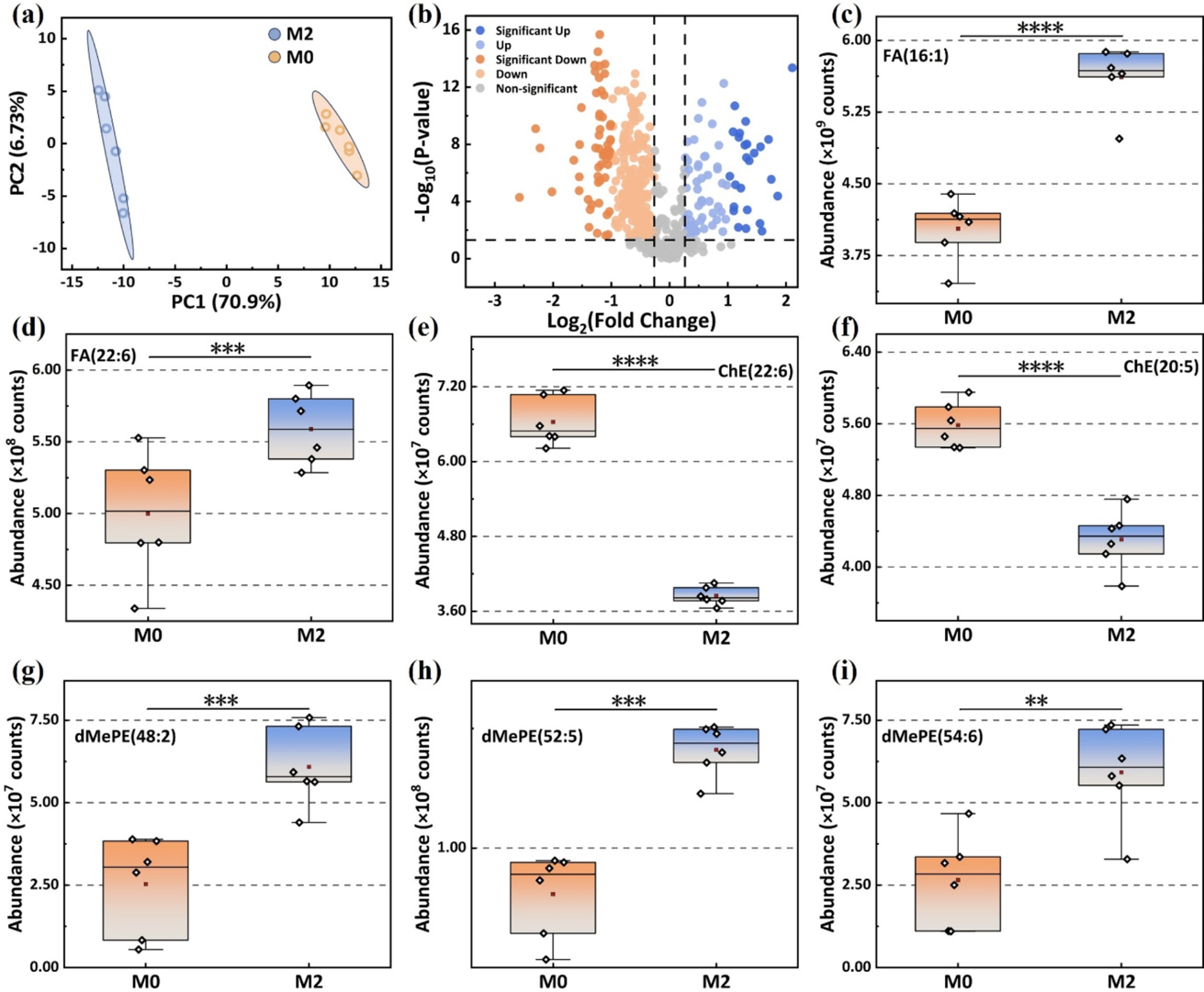
图 5.(a, b) M0 和 M2 小鼠巨噬细胞 EV 中脂质的主成分分析(PCA)和火山图;(c, d) M2 巨噬细胞 EV 中棕榈油酸(FA(16:1))和二十二碳六烯酸(DHA)(FA(22:6))的丰度上调;(e, f) M2 巨噬细胞 EV 中胆固醇酯(CE)水平显著降低;(g - i) M2 巨噬细胞 EV 中二甲磷脂酰乙醇胺(dMePE)上调。
这些微观层面上的脂质重塑,完美呼应了M2型巨噬细胞在宏观上“平息炎症、促进修复”的生理学角色。这不仅为理解免疫代谢机制提供了全新的分子证据,更直接证明了该分析平台在处理稀有细胞样本时无可替代的优势。
见微知著的未来分析范式
这项工作为微量临床样本的深度分子表征打开了一扇新窗。
对于科研工作者与检验医学从业者而言,将繁复的外泌体分离与脂质提取过程浓缩于一张卡片大小的微流控芯片上,绝不仅是工程技术上的炫技。它切实解决了传统流程中死体积大、样本损耗高、人工操作易波动的核心痛点。随着数字微流控硬件的普及与底层算法的优化,这种兼具高时效性与高保真度的“滴血验毒”式微型化工作流,有望在不久的将来成为免疫代谢研究、罕见病标志物筛选以及液体活检领域的主流标配工具。
相关产品介绍: DropletBot®数字微流控平台是一款基于介电润湿原理(EWOD)的电操控数字微流控技术(DMF)的自动化系统 ,通过改变疏水表面上液滴的接触角,精确控制电极阵列表面的离散液滴,广泛应用于生物、化学领域,如诊断、细胞实验和化学合成。DropletBot®具备模块化设计、直观用户界面,能驱动多个独立通道,并提供动态阻抗感应,实现液滴位置、速度和电静力的实时测量。
DropletBot®数字微流控平台是一款基于介电润湿原理(EWOD)的电操控数字微流控技术(DMF)的自动化系统 ,通过改变疏水表面上液滴的接触角,精确控制电极阵列表面的离散液滴,广泛应用于生物、化学领域,如诊断、细胞实验和化学合成。DropletBot®具备模块化设计、直观用户界面,能驱动多个独立通道,并提供动态阻抗感应,实现液滴位置、速度和电静力的实时测量。
参考文献:Menglei Zhao, Hang Li, Yudan Ma, et al. Streamlined Digital Microfluidics-Mass Spectrometry Strategy for Extracellular Vesicle Enrichment and Lipid Profiling. Analytical Chemistry (2026). DOI: 10.1021/acs.analchem.5c07527
原文链接:https://doi.org/10.1021/acs.analchem.5c07527






 粤公网安备44030002004557号
粤公网安备44030002004557号
